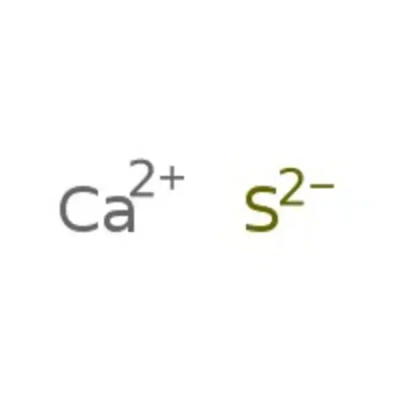Objectifs⚓
Donner des exemples de composés purement covalents.
Donner le nom et la formule de quelques molécules usuelles \((H_2,O_2,Cl_2,N_2,H_2O,HCl,NH_3,CO_2...)\).
Représenter la formule développée et/ou le schéma de Lewis de quelques molécules simples.
Citer des exemples de molécules à caractère ionique partiel.
Citer des exemples de composés ioniques \((NaCl)\).
Donner le nom et la formule statistique de quelques composés ioniques \((NaCl,CaCO_3)\).
Matériel⚓
Vidéo projecteur
Smartphone
Modèles moléculaires
Vérification prérequis⚓
Déroulement⚓
Visionnes attentivement la vidéo ci-dessous, puis réponds aux questions suivantes :
Comment les atomes se lient-ils les uns les autres pour donner des « assemblages » ?
Ces « assemblages » se font-ils de la même manière ?
Quelle est la composition primitive de l'atmosphère terrestre ? Comment a-t-elle évolué avec l'apparition de la vie sur Terre ?
Nota Bene :
Certaines réponses, aux questions posées, seront apportées au fur et à mesure du déroulement du cours.
I. SCHEMA DE LEWIS D'UN ATOME⚓
Le schéma de Lewis d'un atome permet de représenter la structure électronique externe de l'atome en doublets électroniques (représentés par des tirets) et électrons célibataires (représentés par des points isolés).
Rappel :
Les atomes des éléments du groupe (0) sont particulièrement stables.
Il est par contre très rare de trouver les atomes des autres éléments à l'état libre : ils se lient les uns aux autres pour donner des « édifices » stables.
Attention :
Les liaisons entre atomes font intervenir uniquement les électrons des couches externes.
Nota Bene :
Les électrons célibataires sont généralement ceux qui interviennent au niveau des liaisons.
Exemple :
Schémas de Lewis de quelques atomes :
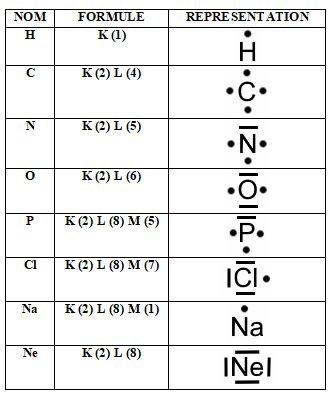
II. LIAISON DE COVALENCE⚓
II.1. Généralisation⚓
La liaison covalente entre 2 atomes est obtenue par une mise en commun de 2 électrons célibataires.
Nota Bene :
Les 2 électrons mis en commun constituent un doublet électronique liant.
Complément : Valence d'un atome
Un atome peut établir autant de liaisons covalentes qu'il a d'électrons célibataires.
La valence d'un atome est égale au nombre de liaisons qu'il peut réaliser.
Exemple :
Le carbone est tétravalent, l'azote est trivalent, l'oxygène est bivalent, l'hydrogène et le chlore sont monovalents.
Définition :
Une molécule est une entité chimique électriquement neutre formée d'un nombre limité d'atomes liés par covalence.
Attention :
Dans une molécule chaque atome possède une couche externe saturée.
Chaque doublet électronique liant est considéré comme appartenant entièrement à chacun des 2 atomes liés.
La représentation de la molécule avec tous les électrons des couches externes des atomes est le schéma de Lewis de la molécule.
II.2. Liaison covalente simple⚓
Mise en commun d'une seule paire d'électrons (un seul doublet liant) entre 2 atomes.
Exemple : Schéma de Lewis de la molécule d'éthanol
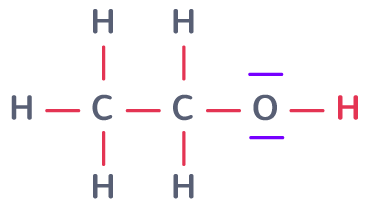
Nota Bene :
La molécule d'éthanol a pour formule brute : \(C_2H_6O\)
II.3. Liaison covalente multiple⚓
II.3.1. Liaison covalente double⚓
Mise en commun de deux paires d'électrons (deux doublets liants) entre 2 atomes.
Exemple : Schéma de Lewis de la molécule de méthanal
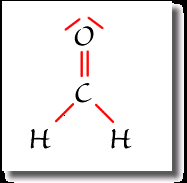
Nota Bene :
Le méthanal a pour formule brute \(CH_2O\)
II.3.2. Liaison covalente triple⚓
Mise en commun de 3 paires d'électrons (trois doublets liants) entre 2 atomes.
Exemple : Schéma de Lewis de la molécule de diazote

Nota Bene :
Le diazote a pour formule brute \(N_2\)
Conseil :
La représentation de la molécule sans les doublets non liants est la formule développée de la molécule.
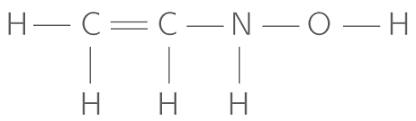
II.4. Liaison covalente dative, liaison covalente polarisée⚓
II.4.1. Liaison covalente dative⚓
Dans une liaison covalente dative un atome, n'ayant pas d'électron célibataire, met en commun un ou plusieurs de ses doublets électroniques libres (non liants) avec un atome ayant une couche externe saturée.
Rappel :
La liaison covalente dative est une liaison covalente dans laquelle les 2 électrons du doublet liant sont fournis par un seul atome.
Nota Bene :
La liaison covalente dative dés qu'elle est établie ne se distingue plus des liaisons covalentes normales.
II.4.2. Liaison covalente polarisée⚓
Une liaison covalente est dite polarisée lorsqu'elle s'établit entre 2 atomes d'électronégativités différentes.
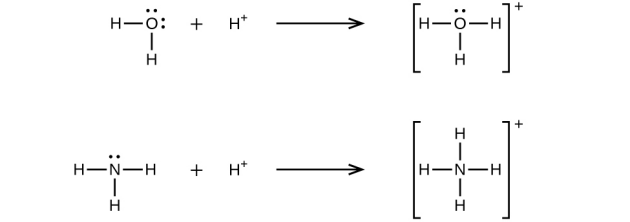
Exemple : Schéma de Lewis de la molécule polarisée de l'eau
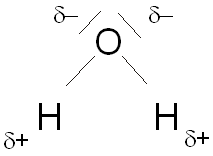
Nota Bene :
L'atome le plus polarisé porte une charge partielle (\(\delta ^-\)), l'autre porte une charge partielle positive (\(\delta ^+\))
III. LIAISON IONIQUE⚓
III.1. Généralisation⚓
La liaison ionique consiste en un transfert d'électrons d'atomes métalliques en général vers des atomes non métalliques de manière à ce que chaque atome acquiert une couche externe saturée.
Nota Bene :
Les ions ainsi obtenus sont étroitement liés par interaction électrostatique.
Définition :
Un solide ionique est toujours formé d'un assemblage de cations et d'anions. L'ensemble est électriquement neutre.
Attention :
On convient d'écrire la formule statistique d'un composé ionique sans indiquer les charges des ions. Cette formule fait intervenir les symboles des éléments affectés en indice de coefficients entiers (les plus petits possibles) traduisant la neutralité électrique.
Complément :
Les ions \(Na^+,\ Cl^-,\ K^+.....\) sont dits monovalents, \(Ca^{2+},\ Mg^{2+},\ O^{2-}...\) sont dits bivalents.
Un ion polyatomique est un groupement d'atomes liés par covalence généralement. L'ensemble a globalement gagné ou perdu un ou plusieurs électrons. Exemples : ion hydronium (\(H_3O^+\)) ; ion hydroxyde (\(HO^-\)) ; ion nitrate (\(NO_3^-\)) ; ion sulfate (\(SO_4^{2-}\)) ; ion ammonium (\(NH_4^+\)) ; ion carbonate (\(CO_3^{2-}\)) ; ion phosphate (\(PO_4^{3-}\)) .
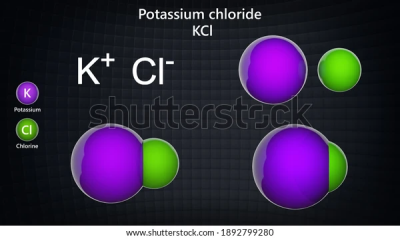
III.1. Exemple 1 : le chlorure de potassium⚓
Le potassium appartient au groupe I (il a 1électron sur sa couche externe).
Le chlore appartient au groupe VII (il a 7électrons sur sa couche externe).
Le potassium a tendance à perdre 1électron pour donner un ion positif \(K^{+}\).
Le chlore a tendance à gagner 1 électron pour donner un ion négatif \(Cl^{-}\).
Nota Bene :
Le chlorure de potassium est un composé ionique de formule ionique (\(K^{+}+Cl^{-}\)) : sa formule statistique est KCl.
III.2. Exemple 2 : le sulfure de calcium⚓
Le calcium appartient au groupe II (il a 2 électron sur sa couche externe).
Le soufre appartient au groupe VI (il a 6 électrons sur sa couche externe).
Le calcium a tendance à perdre 2 électrons pour donner un ion positif \(Ca^{2+}\).
Le soufre a tendance à gagner 2 électrons pour donner un ion négatif \(S^{2-}\).
Nota Bene :
Le sulfure de calcium est un composé ionique de formule ionique (\(Ca^{2+}+S^{2-}\)) : sa formule statistique est \(CaS\).
III.3. Exemple 3 : le sulfate d'aluminium⚓
Le solide ionique de sulfate d'ammonium est constitué d'ions sulfate (\(SO_4^{2-}\)) et d'ions ammonium (\(NH_4^+\)).
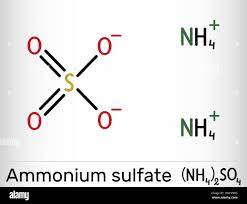
Nota Bene :
Le sulfate d'ammonium est un composé ionique de formule ionique (\(2NH_4^++SO_4^{2-}\)) : sa formule statistique est \(\left(NH_4^{ }\right)_2SO_4\).
TESTS⚓
Test 1⚓
Test 2⚓
Consigne
Ranges dans la cible (molécules ou solides ioniques) qui convient les étiquettes des composés suivants de formule brute :
molécules ou solides ioniques
Test 3⚓
Consigne
Complètes les phrases suivantes en utilisant les mots ou groupes de mots qui conviennent dans le menu déroulant (flèche de défilement).